Stimplus
https://www.stimpluspro.com/FDA/k041359.pdf ![]()
Dear Ms. Preston:
We have reviewed your Section 510(k) premarket notification of intent to market the device referenced above and have determined the device is substantially equivalent (for the indications
for use stated in the enclosure) to legally marketed predicate devices marketed in interstate commerce prior to May 28, 1976, the enactment date of the Medical Device Amendments, or to devices that have been reclassified in accordance with the provisions of the Federal Food, Drug,
and Cosmetic Act (Act) that do not require approval of a premarket approval application (PMA). You may, therefore, market the device. subject to the general controls provisions of the Act.
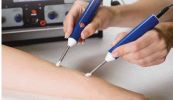
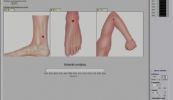
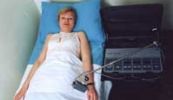
Stimplus adverteert met een serieus ogende brief van de FDA en Stimplus kan ook onaantoonbare acupunctuurpunten vinden. Heel knap.
Waar komt dan die FDA-permissie vandaan?
Gewoon een juridisch gevolg van de in 1976 ingetreden wet.
Alles wat voor die tijd al bestond of er voldoende op lijkt hoeft niet aan de wet te voldoen.
Iniddels is ook dat gewijzigd en dient de fabrikant medische werkzaamheid inzake de ge-adverteerde resultaten aan te tonen.
Daar zal wel een juridisch geschoolde tekstschrijver op worden gezet.